Covid-19: L’autorité américaine de régulation satisfaite de l’efficacité et la sûreté du Vaccin Pfizer/BioNtech
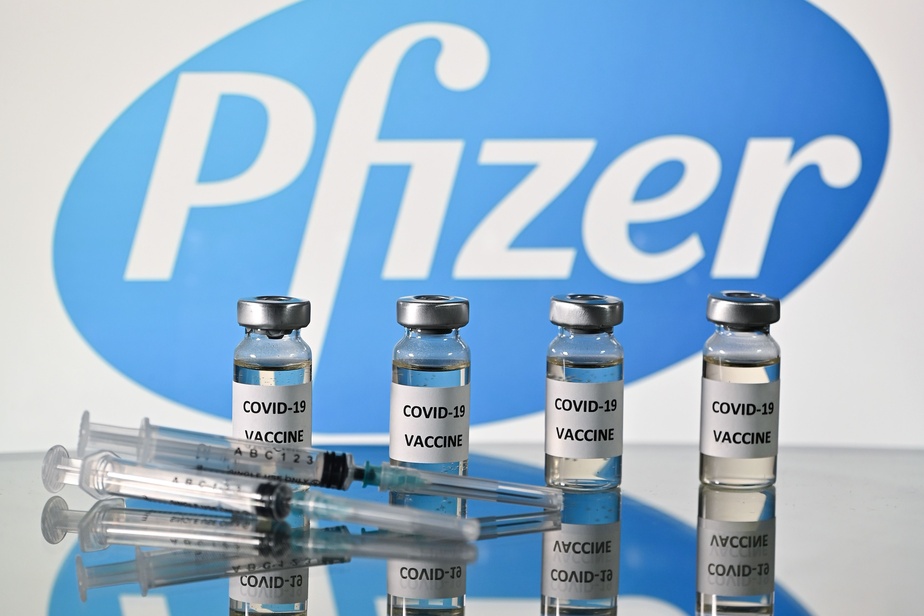
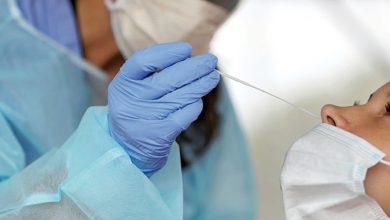
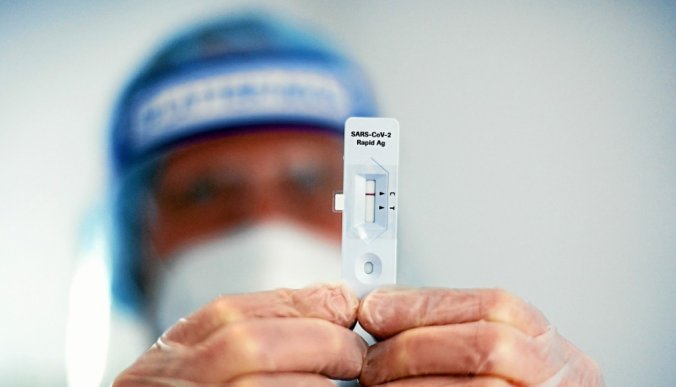
L’autorité de régulation des médicaments aux États-Unis (FDA) a indiqué que le vaccin contre le coronavirus fabriqué par Pfizer et BioNTech offre une forte protection contre le Covid-19 dans les 10 jours environ suivant la première dose, ouvrant la voie à son autorisation d’ici la fin de la semaine.
Selon des documents publiés mardi à la veille d’une réunion de son comité consultatif sur les vaccins, la FDA a précisé que les données issues des essais cliniques « suggèrent un profil de sécurité favorable, sans identification de problème de sécurité spécifique qui empêcherait » l’autorisation en urgence.
Le comité consultatif se réunit jeudi pour discuter de ces conclusions avant le vote sur l’opportunité de recommander de lui accorder le feu vert.
Le géant pharmaceutique américain Pfizer et son partenaire allemand BioNTech avaient lancé un essai clinique à grande échelle en juillet, recrutant 44 000 personnes aux États-Unis, au Brésil et en Argentine. La moitié des volontaires ont reçu le vaccin et la moitié le placebo. En novembre dernier, les deux compagnies ont annoncé que leur vaccin à deux doses avait un taux d’efficacité de 95% après deux doses administrées à trois semaines d’intervalle. Les nouvelles analyses montrent que la protection commence bien plus tôt. « De plus, le vaccin a bien fonctionné indépendamment de la race, du poids ou de l’âge du volontaire. Bien que l’essai n’ait trouvé aucun événement indésirable grave causé par le vaccin, de nombreux participants ont éprouvé des douleurs, de la fièvre et d’autres effets secondaires », selon les mêmes données rapportées par le New York Times.
Confrontés à une nouvelle explosion de cas et d’hospitalisations, les Etats-Unis comptent autoriser ce vaccin dès le feu vert du comité consultatif de l’Agence des médicaments. « Dans les 24 heures suivant le feu vert et l’autorisation de la FDA, nous allons déployer (le vaccin) dans tous les États et territoires », a déclaré le secrétaire américain à la Santé Alex Azar.
Il a déclaré que le même calendrier serait suivi pour l’autre vaccin développé par Moderna, au terme de la réunion de la FDA prévue le 17 décembre. Le gouvernement américain table sur l’obtention du feu vert par plusieurs vaccins afin de déployer près de 40 millions de doses d’ici la fin de cette année. Pour sa part, le Dr Moncef Slaoui, conseiller scientifique en chef de l’opération « Warp Speed » du gouvernement américain, a déclaré que les personnes les plus fragiles pourraient obtenir le vaccin en janvier et février mais la population en général attendra plus longtemps. « Pour que nos vies reviennent à la normale, nous parlons d’avril ou de mai », a-t-il déclaré.
( Avec MAP )