Vaccin Covid-19: les campagnes sont lancées, des questions restent posées
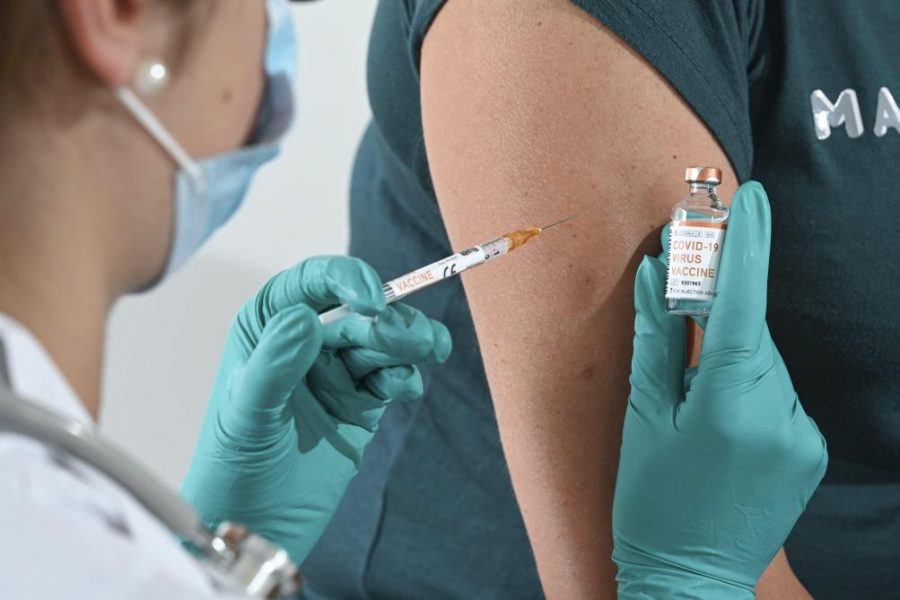
Avec le feu vert accordé par les autorités sanitaires européennes, les campagnes de vaccination vont pouvoir commencer dès dimanche en Europe continentale, après l’Angleterre et les Etats-Unis. Un an seulement après l’apparition du Covid-19, son antidote est disponible, mais des questions demeurent.
Le développement et la mise sur le marché d’un nouveau vaccin prennent d’habitude dix ans en moyenne, un délai réduit à moins d’un an pour le Covid-19, grâce à l’accélération des procédures de recherche, de production industrielle et d’évaluation, appuyée par des financements colossaux.
Le Royaume-Uni a donné le premier feu vert le 2 décembre au vaccin développé par l’américain Pfizer et l’allemand BioNTech. Deux semaines plus tard, près de 138.000 personnes âgées ou personnels sanitaires avaient reçu leur première dose.
Aux Etats-Unis, des autorisations d’urgence ont été accordées par l’Agence américaine des médicaments (FDA) à Pfizer/BioNTech et à Moderna. Le gouvernement prévoit que 20 millions de personnes soient vaccinées d’ici la fin de l’année ou la première semaine de janvier.
Au total, 16 pays et l’Union européenne ont donné leur feu vert au vaccin Pfizer/BioNTech.
De son côté, la Russie a démarré sa campagne le 5 décembre avec le vaccin russe Spoutnik V, encore dans sa troisième et dernière phase d’essais cliniques.
Enfin, les autorités chinoises ont déjà donné leur feu vert à une utilisation d’urgence de certains de leurs vaccins, même si aucun n’a encore été formellement approuvé.
Au total, 14 vaccins en sont au dernier stade de développement, la phase 3, selon le dernier point de l’OMS jeudi dernier, un décompte incluant ceux déjà sur le marché.
Parmi eux se trouvent quatre vaccins chinois ainsi que celui de Johnson & Johnson, qui pourrait demander une autorisation de commercialisation aux Etats-Unis fin janvier ou début février.
Mais au total, 56 « candidats vaccins » sont testés dans des essais cliniques sur l’homme à travers le monde et l’OMS comptabilise 166 projets en phase pré-clinique.
Après l’avis favorable de l’Agence européenne des médicaments (EMA) pour la commercialisation du vaccin Pfizer/BioNTech lundi, la présidente de la Commission européenne, Ursula von der Leyen, a indiqué que la campagne devrait commencer à partir de dimanche. A compter de l’autorisation de mise sur le marché, chaque pays membre reprend la main pour définir les publics prioritaires et l’organisation logistique.
En France, un avis formel de la Haute autorité de santé (HAS) est nécessaire. Il interviendra jeudi, à la veille de Noël.
L’EMA examinera le 6 janvier le dossier de l’Américain Moderna.
Depuis le 9 novembre, quatre fabricants ont annoncé que leur vaccin était efficace: Pfizer/BioNTech, Moderna, l’alliance britannique AstraZeneca/Université d’Oxford, et l’institut d’Etat russe Gamaleïa.
Ces annonces s’appuient sur le dernier stade des essais cliniques, la phase 3, pour lequel des dizaines de milliers de volontaires ont été recrutés.
Mais les données scientifiques détaillées et validées sont disponibles seulement pour deux d’entre eux: ceux de Pfizer/BioNTech et d’AstraZeneca/Oxford.
La revue scientifique The Lancet a confirmé le 8 décembre que le vaccin d’AstraZeneca était efficace à 70% en moyenne.
Cette efficacité est une moyenne car deux différents protocoles ont été utilisés: certains volontaires ont d’abord reçu une demi-dose, puis une dose complète un mois plus tard, avec une efficacité de 90%. Mais elle descend à 62% pour le reste des volontaires, pourtant vaccinés avec deux doses complètes.
AstraZeneca a reconnu que l’administration d’une demi-dose provenait d’une erreur et a annoncé la tenue d’une « étude supplémentaire » pour vérifier ces résultats.
Pour le vaccin Pfizer/BioNTech, la FDA a confirmé dans un compte-rendu sur les données de l’essai la très haute efficacité à 95% du vaccin, administré en deux doses espacées de trois semaines.
Moderna se prévaut d’une efficacité très proche, de 94,1%. Le vaccin Spoutnik V russe, lui, affiche une efficacité de 91,4% sur ses 39 malades (et 95% sur un nombre de malades non précisé).
Le vaccin AstraZeneca/Oxford a pour lui d’être le moins cher (environ 2,50 euros la dose). Ceux de Moderna et de Pfizer/BioNTech ont un handicap logistique, car ils ne peuvent être stockés à long terme qu’à très basse température (-20° Celsius pour le premier, -70°C pour le second).
Les experts soulignent qu’avec des essais cliniques menés sur des dizaines de milliers de volontaires, un problème majeur de sûreté aurait déjà été détecté. Mais des effets secondaires plus rares ou ne survenant que chez certains profils de patients ne sont pas à exclure.
Selon le rapport de la FDA sur le vaccin Pfizer/BioNTech, ce dernier provoque souvent des réactions douloureuses au niveau de l’injection dans le bras (de l’ordre de 80%). Suivent des effets indésirables tels que fatigue, maux de tête et courbatures, plus rarement de la fièvre.
Les seuls effets indésirables graves que la FDA estime potentiellement causés par l’administration du vaccin sont au nombre de deux: une blessure à l’épaule liée à l’injection, et un cas de gonflement des ganglions. Quelques cas de grave réaction allergique ont aussi été signalés.
La plus importante est celle de l’efficacité à long terme, puisque pour l’instant elle a été calculée une à deux semaines seulement après la dernière injection.
« Combien de temps la protection durera-t-elle? Le virus finira-t-il par muter pour échapper au vaccin, ce qui limiterait alors l’efficacité de la vaccination? », résume une experte britannique, Penny Ward (King’s College de Londres), citée par l’organisme Science Media Centre (SMC).
Autre question cruciale: on ignore si l’action de ces vaccins est identique chez les populations les plus à risque, à commencer par les personnes âgées, qui sont plus susceptibles de développer une forme grave.
Il reste aussi à savoir si ces vaccins font barrage à la transmission du virus, en plus de réduire la sévérité de la maladie chez ceux qui les ont reçus.
Les experts de l’Union européenne estiment que les vaccins actuels contre le Covid-19 restent efficaces face à la nouvelle souche du virus détectée au Royaume-Uni, présentée comme plus contagieuse par les Britanniques.
« Pour le moment il n’existe aucune preuve suggérant » que le vaccin Pfizer/BioNTech « ne soit pas efficace contre le nouveau variant », a déclaré l’Agence européenne du médicament. Un message répété par le co-dirigeant du laboratoire allemand BioNTech, Ugur Sahin, qui a également assuré que son entreprise était en mesure de délivrer un nouveau vaccin en six semaines.
( Avec AFP )






